 Limited Edition Golden Llama is here! Check out how you can get one.
Limited Edition Golden Llama is here! Check out how you can get one.  Limited Edition Golden Llama is here! Check out how you can get one.
Limited Edition Golden Llama is here! Check out how you can get one.
 Offering SPR-BLI Services - Proteins provided for free!
Offering SPR-BLI Services - Proteins provided for free! Get your ComboX free sample to test now!
Get your ComboX free sample to test now!
 Time Limited Offer: Welcome Gift for New Customers !
Time Limited Offer: Welcome Gift for New Customers !  Shipping Price Reduction for EU Regions
Shipping Price Reduction for EU Regions
> Materias primas claves para la terapia celular y genética
ACROBiosystems ofrece una amplia gama de materias primas y herramientas necesarias para los productos de terapia celular, incluyendo citoquinas, nucleasas y perlas de activación. Proporcionamos varios grados de materiales, incluidos los de primera calidad y los de GMP. Nuestras proteínas de primera calidad proceden del mismo clon, secuencia y sistema de expresión que nuestros productos GMP. Esto significa que los desarrolladores que utilizan nuestros productos de primera calidad pueden pasar fácilmente a productos GMP para su uso en etapas CMC o clínicas sin más estudios de comparabilidad del proceso de fabricación.
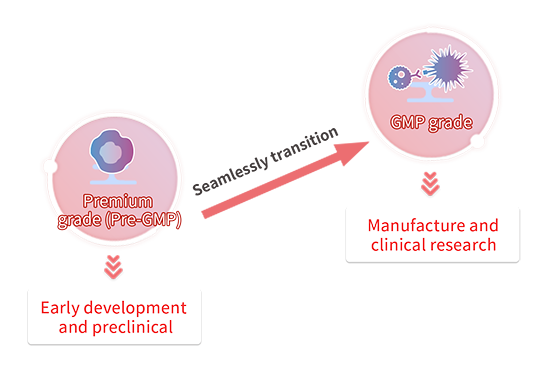
Para facilitar la transición de su producto de terapia celular a los ensayos clínicos y más allá, es fundamental desarrollar una estrategia de materias primas que tenga en cuenta el objetivo final. Para la investigación y el desarrollo de la terapia celular en su fase inicial, lo más habitual es utilizar materiales de uso exclusivo en investigación (RUO). Sin embargo, a medida que el desarrollo avanza hacia las fases preclínicas o clínicas, los materiales RUO que antes podían ser suficientes no cumplen los criterios necesarios para seguir adelante. La mayoría de las estrategias hacen hincapié en el uso de las materias primas de mayor calidad disponibles lo antes posible; sin embargo, esto no siempre es factible. Tener en cuenta las transiciones de grado de los materiales puede ayudar a equilibrar tanto el rendimiento como los costes al pasar a la siguiente fase.
ACROBiosystems ofrece diferentes grados de materiales para diferentes etapas de desarrollo de su producto de terapia celular. Los materiales de primera calidad se producen bajo nuestro riguroso sistema de control de calidad, que incorpora un amplio conjunto de pruebas, incluidas las de esterilidad y endotoxinas. El rendimiento del producto se valida cuidadosamente y se comprueba su compatibilidad para el uso en cultivos celulares o cualquier otra aplicación en la fase preclínica temprana. Cuando esté listo para pasar a fases clínicas posteriores, también ofrecemos un servicio de proteínas GMP personalizado que se adapta a sus necesidades. Los materiales de grado GMP se desarrollan utilizando nuestra plataforma de sistema de gestión de calidad de grado GMP. Estos productos se fabrican con una estricta gestión de la calidad y con normas de prueba de liberación de medicamentos. Dado que nuestros componentes de grado Premium(Pre-GMP) son similares a nuestros productos GMP, la transición entre grados puede realizarse fácilmente sin necesidad de más estudios de comparabilidad.
| Premium(Pre-GMP) Grade | GMP Grade | |
|---|---|---|
| Application | Research and Development; Preclinical research, seamless transition into clinical phases | Designed to meet clinical phase requirements and bolster your IND application to various regulatory bodies. |
| Quality System | ISO 9001 /ISO 13485 Certified | ISO 9001 /ISO 13485 Certified (Development stage) GMP Quality Management System (Production stage) |
| Production | ISO certified facilities | GMP certified facilities -by third-party audits |
| Transient or stable cell lines | Stable cell lines (Comprehensive external inspections) | |
| Animal-origin free materials or BSE/TSE free | Animal-origin free materials or BSE/TSE free | |
| Pharmaceutical-grade materials | Pharmaceutical-grade materials | |
| Strict 2 grade series sterile filtration | Strict 2 grade series sterile filtration | |
| Class 100 FFU | Class B+A cleanroom with automatic filling machine | |
| No additional virus clearance steps in | 2 additional virus removal and inactivation steps included (nanofiltration + low pH) | |
| Quality Control | Sterility / Mycoplasma testing | Sterility / Mycoplasma testing |
| Endotoxin control and detection | Endotoxin control and detection | |
| Validated key equipment and analytical instruments | Validated equipment /analytical instruments/analytical methods(analytical instruments audit trial) | |
| Residual DNA/HCP testing | Residual DNA/HCP testing | |
| Limited adventitious agent testing | Full adventitious agent testing (virus testing and animal in vivo safety experiments) | |
| Documentation | Common regulatory support | Comprehensive regulatory support files |
| DMF filing (Few products) | DMF filing (All products) |
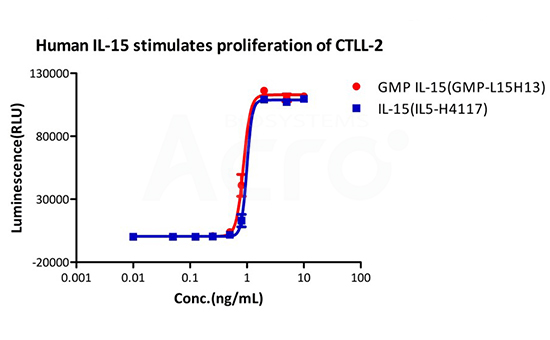
Recombinant Human IL-15 Protein premium grade (IL5-H4117), designed for preclinical stage, has the same activity and performance with GMP Grade IL-15 (GMP-L15H13), which enables a seamless transition from preclinical development to clinical phases .
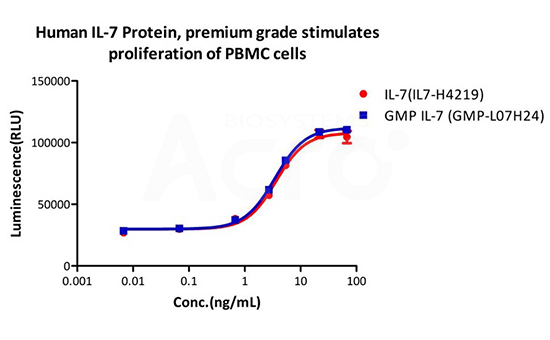
Human IL-7 Protein premium grade (IL7-H4219) designed for preclinical stage, has the same activity and performance with GMP Grade IL-7 (GMP-L07H24), which enables a seamless transition from preclinical development to clinical phases .
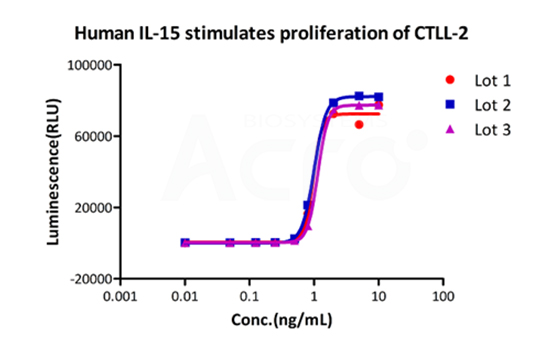
Bioactivity of three different lots of GMP Human IL-15 (GMP-L15H13) verified by cell-based assay, and the result shows very high batch-to-batch consistency.
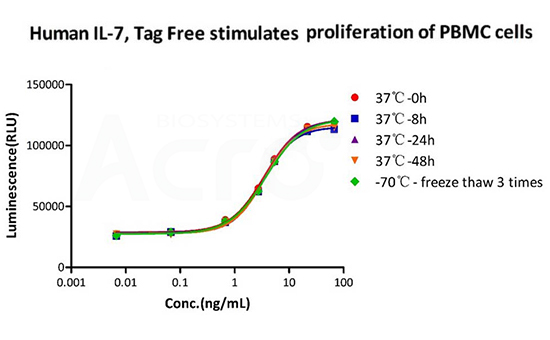
The Cell based assay shows that GMP Human IL-7 (GMP-L07H24) is stable at 37°C for 48 hours and after freezing and thawing 3 times.
This web search service is supported by Google Inc.
